首项结果!用瑞德西韦后68%新冠病人好转 在华重症研究终止
备受关注的瑞德西韦(Remdesivir)治疗新冠肺炎的首个临床研究结果4月10日公布。在53名来自全球的患者中,36人(约占68%)获得了临床改善。
瑞德西韦是一款在研药物,前期主要用于治疗埃博拉和中东呼吸综合征等疾病,目前还未在全球任何一个国家获批上市。
此前,美国首例新冠肺炎确诊患者在接受了瑞德西韦治疗后症状出现了立竿见影的改善,随后该药受到广泛关注。

吉利德科学3月份提供的在美国制造的瑞德西韦的照片。(图片来源:吉利德科学/美联社)
53名来自全球的患者接受同情用药,非临床试验
上海澎湃新闻报道,吉利德科学公司(Gilead Sciences)10日在顶级医学期刊《新英格兰医学杂志》(NEJM)上发布了瑞德西韦治疗新冠肺炎(COVID-19)的首个临床研究结果。
研究显示,53名新型冠状病毒肺炎严重并发症的住院患者,以个例同情用药的方式接受了在研抗病毒药物瑞德西韦的治疗。这53名来自全球的患者中,36人(约占68%)获得了临床改善。
值得注意的是,在首批公布的临床数据中,总计32名患者(约占60%)出现副作用,最常见的是肝脏酶指标升高、腹泻、皮疹、肾功能障碍和高血压。
总计12名(23%)患者出现严重副作用,其中包括多器官多器官功能障碍综合征、败血性休克、急性肾脏损伤和高血压。
另外,接受治疗的53名患者中,有7名在完成瑞德西韦治疗后死亡,其中包括6名接受有创通气的患者和1名接受无创氧气支持的患者。
上述结果公布以后,引发业界的讨论。有一种观点认为,由于样本数据量过小,且无对照组数据,这一结果的实际意义值得商榷。
吉利德科学11日在中国官网公布了该公司董事长兼首席执行官丹尼尔·奥戴(Daniel O’Day)的公开信。
信中说,这些患者是无法参加临床试验的危重患者,通过同情用药程序,他们接受了瑞德西韦的治疗。单纯从研究角度来看,这些同情用药的数据存在局限性,
然而,这些数据对于获得了症状改善的患者来说有着非常大的意义。这53名患者的早期数据并非通过临床试验获得,且数据只覆盖了少数接受瑞德西韦治疗的危重患者。
人民日报健康客户端报道,北京医院药学部副主任药师张亚同介绍:“同情用药是允许给一些不符合批准的临床条件,但无药可救的患者,在开展临床试验时,使用尚未得到批准上市的药物。”
在中国进行的一系列研究中,新冠重症患者的死亡率在17%-78%之间,与这些数字相比,该研究提供了瑞德西韦治疗重症患者13%的死亡率的最新数据,值得关注。
张亚同称,对于瑞德西韦有效性及安全性研究,有待进一步临床研究。
全球共有7项研究 中国针对重症患者的研究已停止
丹尼尔·奥戴的公开信中透露,中国针对重症患者的研究已停止。
关于临床试验,信中说,有7项临床试验已经启动。中国在2月初启动了最早的两项对重症和中症患者的研究。此后,新增的5项试验在世界各地启动。
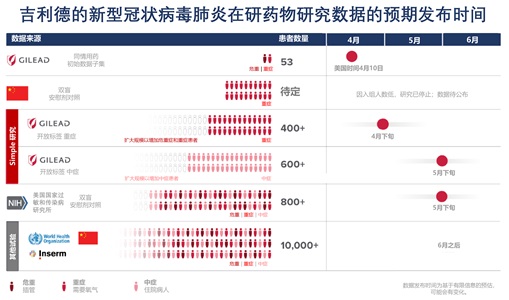
瑞德西韦各项试验的汇总和预期的数据公布时间。(图片来源:吉利德科学官网)
吉利德正在美国、亚洲和欧洲的新型冠状病毒肺炎高发地区进行两项三期研究。其中一项研究针对重症患者,另一项研究针对中症患者。
美国国家过敏和传染病研究所(NIAID)于2月21日开始了一项全球试验。该试验将随机分配患者使用瑞德西韦或安慰剂,以对照比较试验结果。该试验正在入组约800名具有不同症状的患者。
世界卫生组织也在进行一项全球试验,名为Solidarity,Inserm DisCoVeRy试验最近已在欧洲开始。
信中透露,预计在4月底获得瑞德西韦针对重症患者研究的初步数据。中国的研究者将负责发布瑞德西韦在中国的试验数据,
但是,因入组停滞,针对重症患者的研究已停止。预计5月份获得有安慰剂对照的NIAID试验的初步数据,以及吉利德的针对中度症状新型冠状病毒肺炎患者的研究数据。